SOONCHUNHYANG INDUSTRY-ACADEMY COOPERATION FOUNDATION
[순천향대 김우태 교수]
ATR 활성화 기전 규명으로 유전체 안정성 유지 역할 밝혀
순천향대(총장 송병국) 의생명연구원 김우태 교수 연구팀이 항암 치료와 항암제 내성 극복의 새로운 가능성을 제시하는 연구 성과를 발표했다. 연구진은 PHRF1 단백질이 ATR(Ataxia Telangiectasia and Rad3-related) 활성화를 촉진하여 유전체 안정성을 유지하는 새로운 분자 기전을 규명했다고 밝혔다.
세포는 자외선, 방사선, 화학물질 등 외부 환경뿐만 아니라 내부 대사 과정에서도 지속적으로 DNA 손상을 겪는다. 이러한 손상이 적절히 복구되지 않으면 유전체 불안정성이 증가하고, 암과 같은 질병의 원인이 될 수 있다. 이를 방지하기 위해 세포는 DNA 손상 수복(DNA Damage Response, DDR) 시스템을 활성화하여 손상된 DNA를 복구하고 유전체를 보호하는 기능을 수행한다.
특히 ATR은 DDR 과정에서 중요한 역할을 하는 단백질로, DNA 복제 과정에서 발생하는 손상을 감지하고 복구 신호를 전달하여 세포 주기를 조절하는 기능을 한다. ATR의 활성화를 위해서는 TopBP1 단백질과의 상호작용이 필수적인데, 이번 연구에서는 PHRF1이 TopBP1의 단일 유비퀴틴화(mono-ubiquitination)를 유도하여 ATR 활성화를 촉진한다는 사실이 밝혀졌다.
김우태 교수 연구팀은 PHRF1이 E3 유비퀴틴 리가아제로 작용하여 TopBP1에 단일 유비퀴틴을 추가하면 ATR 활성화 기능이 향상된다는 점을 확인했다. 이를 통해 DDR이 효과적으로 유도되며, 결과적으로 유전체 안정성이 유지될 수 있다는 것이 이번 연구의 핵심이다.
이러한 연구 성과는 항암 치료 전략에도 중요한 의미를 갖는다. ATR은 다양한 암세포에서 활성화되는 DDR 경로이지만, 특정 암에서는 DDR 기능이 손상되거나 ATR 경로에 의존하는 특성을 보인다. 이에 따라 ATR을 표적으로 하는 항암제 개발이 활발히 진행되고 있으며, 이번 연구에서 밝혀진 PHRF1-TopBP1-ATR 축이 새로운 치료 표적으로 활용될 가능성이 주목받고 있다.
연구를 주도한 김우태 교수는 "이번 연구를 통해 ATR 활성화의 새로운 조절 메커니즘을 규명했다"며 "향후 이 경로를 활용한 항암 치료 전략이 개발된다면 기존 항암제에 대한 내성을 극복하는 데 기여할 수 있을 것"이라고 밝혔다.
이번 연구는 한국연구재단 중견연구자 지원사업, 오믹스 기반 정밀의료기술 개발사업 및 순천향대학교의 지원을 받아 수행되었으며, 국제학술지 Nucleic Acids Research (Impact Factor 16.7, BIOCHEMISTRY & MOLECULAR BIOLOGY 분야 상위 1.71%, 2023 JCR 기준) 2025년 3월호에 게재되었다.
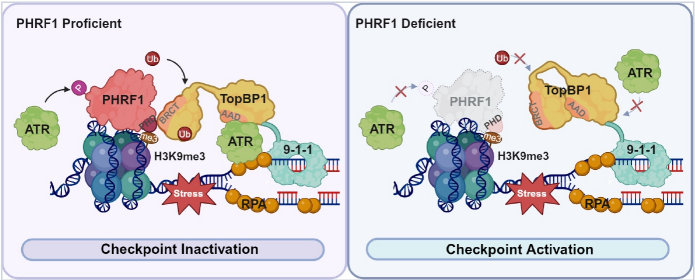
[유전체 안전성 유지 모식도]


